Tekst opublikowany w czasopiśmie „Niedziałki” w 2012 roku. Opublikowano za zgodą redakcji czasopisma. Do napisania artykułu skłoniło mnie zadanie maturalne z 2011 roku, które znacznie utrudniło życie wielu maturzystom.
Paweł Bernard Niedziałki 1/2012, s.10-16
Wstęp
Egzamin maturalny z chemii na poziomie rozszerzonym w roku 2010/2011 nie należał do najłatwiejszych, a dodatkowo wzbudził sporo kontrowersji. Oto jedno z pytań, które sprawiło wiele kłopotów [1]:
| Zadanie 14. (4 pkt) Poniżej przedstawiony jest schemat reakcji:
MnO42- + H+ → MnO4− + MnO2 + H2O
a) Napisz w formie jonowej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równania procesów redukcji i utleniania zachodzących podczas tej przemiany.
Równanie reakcji redukcji: ……………………………………………………………………………..
Równanie reakcji utleniania: …………………………………………………………………………..
b) Dobierz i uzupełnij współczynniki stechiometryczne w poniższym schemacie.
………. MnO42- + ………. H+ → ………. MnO4− + ………. MnO2 + ………. H2O
c) Napisz, jakie funkcje pełnią jony MnO42− w tej reakcji. |
W zadaniu uczniowie mieli za zadanie uzgodnić podane równanie reakcji w oparciu o zapisane pełne równania redukcji i utleniania. Ta metoda uzgadniania równań REDOX to tak zwana metoda równań połówkowych. Problem stanowi fakt, iż metoda ta nie jest wyszczególniona w obowiązującej podstawie programowej z chemii [2,3]. Z tego powodu praktycznie w żadnym polskim podręczniku do chemii na poziomie szkoły ponadgimnazjalnej metoda ta nie jest omawiana. Tradycyjnie uzgadnianie równań reakcji utleniania-redukcji opierane jest o bilans elektronowy nazywany równaniami cząstkowymi (często mylonymi z równaniami połówkowymi). Czym zatem różnią się te dwie metody?
Uzgodnienie w oparciu o bilans elektronowy
Uzgodnijmy podane w zadaniu równanie reakcji metodą równań cząstkowych.
1. Należy przypisać pierwiastkom stopnie utlenienia i znaleźć atomy, które ulegają utlenieniu bądź redukcji. W tym przypadku ww. zadania maturalnego zarówno utlenieniu jak i redukcji uległ mangan.
2. Zapisujemy schemat procesów utlenienia i redukcji w oparciu o atomy, które wzięły udział w każdym z tych procesów wraz z podaniem liczby przyjmowanych lub oddawanych elektronów. Liczba przyjętych i oddanych elektronów musi być równa w obu procesach, w tym celu dobierany jest tzw. „mnożnik”.
|
|
|
Mnożnik
|
| VI |
red |
IV |
|
| Mn + 2e– |
→ |
Mn |
1
|
| VI |
utl |
VII |
|
| Mn |
→ |
Mn + 1e– |
2(1)
|
3. Wyznaczony mnożnik stanowi o liczbie atomów każdego typu. Na tej podstawie uczeń jest w stanie zapisać podane równanie reakcji w formie:
3MnO42- + H+ → 2MnO4− + MnO2 + H2O
4. Ponieważ bilans elektronowy został uzgodniony dalsze uzgodnienie równia przeprowadza się w sposób klasyczny.
Metoda ta prowadzi do poprawnego rozwiązania zadania, jednak przedstawione równania cząstkowe nie są pełnymi równaniami reakcji utleniania i redukcji. Z tego powodu rozwiązanie to nie było punktowane.
Uzgodnienie w oparciu o równania połówkowe (równania jonowo-elektronowe)
Jak można wnioskować na postawie samej nazwy, równania połówkowe po zsumowaniu powinny stworzyć pełne równanie analizowanej reakcji chemicznej. Zatem zadanie to mogło być rozwiązane w następujących etapach:
1. Podobnie jak w metodzie bilansu elektronowego należy zacząć od przypisana pierwiastkom stopni utlenienia i znaleźć pierwiastki, które ulegają utlenieniu bądź redukcji. W tym przypadku do opisu procesów zapisujemy nie tylko atomy, których stopień utlenienia uległ zmianie, ale całe indywidua (cząsteczki, jony lub atomy) które biorą udział w reakcji. Zacznijmy od równania, w którym zachodzi redukcja:
| VI |
red |
IV |
| MnO42- + 2e– |
→ |
MnO2 |
2. Równanie połówkowe należy uzgodnić. Nie jest to jednak możliwe wprost, ze względu na różną liczbę atomów tlenu. W takim wypadku po stronie równania, w której występuje deficyt atomów tlenu dopisuje się odpowiednią liczbę cząsteczek wody:
| VI |
red |
IV |
| MnO42- + 2e– |
→ |
MnO2 + 2H2O |
3. Dopisanie cząsteczek wody spowodowało deficyt atomów wodoru po stronie substratów. Deficyt ten uzupełniamy dopisując odpowiednią liczbę kationów wodoru:
| VI |
red |
IV |
|
| MnO42- + 2e– + 4H+ |
→ |
MnO2 + 2H2O |
|
4. W ten sposób równanie redukcji zostało uzgodnione. Kolejnym etapem jest uzgodnienie równania utleniania:
| VI |
utl |
VII |
| MnO42- |
→ |
MnO4− + e– |
5. W tym przypadku liczba atomów po stronie substratów i produktów jest równa. Należy jednak równanie utleniania podwoić, aby liczba oddanych elektronów była zgodna z liczbą elektronów przyjętych podczas procesu redukcji. Następnie sumujemy procesy:
| (1x) |
MnO42- + 2e– + 4H+ |
→ |
MnO2 + 2H2O |
| (2x) |
2MnO42- |
→ |
2MnO4− + 2e– |
| Sumujemy równana stronami |
| 3MnO42- + 4H+ |
→ |
MnO2 + 2H2O + 2MnO4− |
W ten sposób otrzymujemy w pełni uzgodnione równanie. Schemat postępowania, tzn. dopisanie odpowiedniej liczby cząsteczek wody i kationów wodoru jest uniwersalny i znajduje zastosowanie przy uzgadnianiu zarówno równań zapisanych w formie cząsteczkowej jak i jonowej.
W przypadku przedstawionego zadnia maturalnego obie metody prowadziły do tego samego wyniku, zatem narzucenie formy rozwiązania zadania jest mocno kontrowersyjne. Dodatkowo układ graficzny zadania tzn. jedna pusta linia na wpisanie równania redukcji mogła być myląca i z pewnością utrudniała zapis rozwiązania.
Czy zatem stosowanie równań połówkowych jest potrzebne?
Osoba układająca pytanie mogła wymusić sposób rozwiązania zadania inaczej je formując. W treści zadania zamiast podawać pełny schemat mogła zapisać jedynie jego fragment:
MnO42- → MnO4− + MnO2
Oczywiście podniosłoby to poziom trudności zadania, ale rozwiązanie tego przykładu w oparciu o bilans elektronowy nie byłoby możliwe.
Równania połówkowe znajdują często zastosowanie, gdy nie jest znane całe równanie reakcji, a jego zapisy jest opary o obserwacje.
Przykład 1 – klasyczny probierz trzeźwości
Wykrywanie alkoholu w wydychanym powietrzu było dawniej przeprowadzane przez tak zwane „dmuchanie w balonik”. Powietrze z balonika było przepuszczane nad pomarańczowym dichromianem(VI). Zmiana zabarwienia na zieloną związana była z redukcją dichromianu(VI) do związku chromu(III) i jednoczesnym utlenieniem alkoholu do kwasu karboksylowego. Równanie to można zapisać i uzgodnić w oparciu o równania połówkowe:
| VI |
red |
III |
| Cr2O72– |
→ |
2Cr3+ |
| -III – I |
utl |
-III III |
| CH3CH2OH |
→ |
CH3COOH |
Uzgadnianie równania redukcji krok po kroku:
|
VI |
red |
III |
| 1 |
Cr2O72– + 6e– |
→ |
2Cr3+ |
| 2 |
Cr2O72– + 6e– |
→ |
2Cr3+ + 7H2O |
| 3 |
Cr2O72– + 6e– + 14H+ |
→ |
2Cr3+ + 7H2O |
Uzgadnianie równania utleniania krok po kroku:
|
-III – I |
utl |
-III III |
| 1 |
CH3CH2OH |
→ |
CH3COOH + 4e– |
| 2 |
CH3CH2OH + H2O |
→ |
CH3COOH + 4e– |
| 3 |
CH3CH2OH + H2O |
→ |
CH3COOH + 4e– + 4H+ |
Sumaryczne równanie:
| Mnożnik |
|
|
|
|
(2x)
|
2Cr2O72– + 12e– + 28H+ |
→ |
2Cr3+ + 14H2O |
|
(3x)
|
3CH3CH2OH + 3H2O |
→ |
3CH3COOH + 12e– + 12H+ |
| Sumujemy równana stronami |
| 2Cr2O72– + 16H+ + 3CH3CH2OH |
→ |
2Cr3+ + 11H2O + 3CH3COOH |
Przykład 2 – redukcja manganianu(VII)
Fioletowy jon manganianowy(VII) uległ reakcji z siarczanem(IV). W wyniku reakcji powstał bezbarwny roztwór:
| VII |
red |
II |
| MnO4– |
→ |
Mn2+ |
| IV |
utl |
VI |
| SO32– |
→ |
SO42– |
Uzgodnienie równania redukcji krok po kroku:
|
VII |
red |
II |
| 1 |
MnO4– |
→ |
Mn2+ |
| 2 |
MnO4– + 5e– |
→ |
Mn2+ + 4H2O |
| 3 |
MnO4– + 5e– + 8H+ |
→ |
Mn2+ + 4H2O |
Uzgodnienie równania utleniania krok po kroku:
|
IV |
utl |
VI |
| 1 |
SO32– |
→ |
SO42– + 2e– |
| 2 |
SO32– + H2O |
→ |
SO42– + 2e– |
| 3 |
SO32– + H2O |
→ |
SO42– + 2e– + 2H+ |
Sumaryczne równanie:
| Mnożnik |
|
|
|
|
(2x)
|
2MnO4– + 10e– + 16H+ |
→ |
2Mn2+ + 8H2O |
|
(5x)
|
5SO32– + 5H2O |
→ |
5SO42– + 10e– + 10H+ |
| Sumujemy równana stronami |
| 2MnO4– + 6H+ + 5SO32– |
→ |
2Mn2+ + 3H2O + 5SO42– |
Na podstawie zapisanego równania widać, że reakcja zaszła w środowisku kwasowym. Do uzgadniania reakcji biegnących w środowisku zasadowym należy zastosować jedną z alternatywnych metod[4]:
Przykład 3 – redukcja manganianu(VII) w środowisku zasadowym
Redukcja:
|
VII |
red |
VI |
| 1 |
MnO4– + e– |
→ |
MnO42- |
Utlenianie:
|
IV |
utl |
VI |
|
| 1 |
SO32– |
→ |
SO42– + 2e– |
|
| 2 |
SO32– + 2OH– |
→ |
SO42– + 2e– |
Zamiast cząsteczki wody dopisujemy jony OH– (dwa jony na każdy brakujący atom tlenu) |
| 3 |
SO32– + 2OH– |
→ |
SO42– + 2e– + H2O |
Po drugiej stronie równania dopisujemy cząsteczki wody tak, aby zbilansować równanie (jedna cząsteczka na dwa jony OH–) |
| Mnożnik |
|
|
|
|
(2x)
|
2MnO4– + 2e– |
→ |
2MnO42- |
|
(1x)
|
SO32– + 2OH– |
→ |
SO42– + 2e– + H2O |
| Sumujemy równana stronami |
|
|
| 2MnO4– + SO32– + 2OH– |
→ |
2MnO42- + SO42– + H2O |
Co jednak zrobić, gdy środowisko reakcji nie jest zdefiniowane? W taki przypadku możemy zastosować ogólną metodę (przedstawioną w przykładzie 1 i 2):
Redukcja:
|
VII |
red |
VI |
| 1 |
MnO4– + e– |
→ |
MnO42- |
Utlenianie:
|
IV |
utl |
VI |
| 1 |
SO32– |
→ |
SO42– + 2e– |
| 2 |
SO32– + H2O |
→ |
SO42– + 2e– |
| 3 |
SO32– + H2O |
→ |
SO42– + 2e– + 2H+ |
Sumaryczne równanie:
| Mnożnik |
|
|
|
|
(2x)
|
2MnO4– + 2e– |
→ |
2MnO42- |
|
(1x)
|
SO32– + H2O |
→ |
SO42– + 2e– + 2H+ |
| Sumujemy równana stronami |
| 2MnO4– + SO32– + H2O |
→ |
2MnO42- + SO42– + 2H+ |
Zapis równań tą metodą może prowadzić do mylnego wniosku, że reakcja zaszła w środowisku obojętnym. Jednak, bardziej ostrożnie sformułowany wniosek, że pH w trakcie reakcji maleje, jest poprawny. Jeśli na tym etapie zostanie podana informacja, że początkowo pH roztworu było większe niż 7, równanie to można uzupełnić przez zalkalizowanie substratów. Osiągnąć to można stosując prosty zabieg techniczny – zsumowanie równania z równaniem autodysocjacji wody.
| 2MnO4– + SO32– + H2O |
→ |
2MnO42- + SO42– + 2H+ |
| 2H+ + 2OH– |
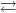 |
2H2O |
| Sumaryczne równanie: |
| 2MnO4– + SO32– + 2OH– |
→ |
2MnO42- + SO42– + H2O |
Ostatecznie obydwie metody dają ten sam rezultat.
Podsumowanie
Równania połówkowe stanowią proste narzędzie pozwalające nie tylko dobrać współczynnik stechiometryczne do równań utleniania-redukcji, ale również uzupełnić równania o niektóre substraty lub produkty i na tej podstawie wnioskować o zmianie odczynu towarzyszącemu reakcji. Przedstawiona metoda uzgadniania równań połówkowych wydaje się nie być trudniejsza od metody bilansu elektronowego. Należy jednak podkreślić, że w przypadku gdy dysponujemy pełnym zapisem schematu reakcji, stosowanie tej metody nie niesie ze sobą korzyści, a może być uznane za dość pracochłonne. Niemiej jednak, mając na uwadze zbliżający się egzamin maturalny, być może warto poświęcić chwilę czasu na lekcji powtórzeniowej na omówienie tej metody, przedyskutowanie jej zalet i rozwiązanie poniższego zadania.
Zadanie
Poniżej przedstawiono zestaw schematów procesów utleniania i redukcji. Połącz procesy w pary i metodą równań połówkowych zapisz i uzgodnij odpowiednie równania reakcji. Uwzględnij wszystkie możliwe kombinacje (UWAGA: rozstrzygnięcie problemu, czy dany proces może zajść w rzeczywistości nie jest przedmiotem rozważań).
- I. Co3+ → Co2+
- II. PbO2 → Pb2+
- III. ClO3– → Cl–
- IV. Sn2+ → Sn4+
- V. NO2 → NO3–
Literatura
1. Egzamin maturalny z chemii, poziom rozszerzony, maj 2011 s. 8
2. Rozporządzenie Ministra Edukacji Narodowej z dnia 23 grudnia 2008 r. w sprawie podstawy programowej wychowania przedszkolnego oraz kształcenia ogólnego w poszczególnych typach szkół Dzienniku Ustaw z dnia 15 stycznia 2009 r. Nr 4, poz. 17
3. Podstawa programowa z komentarzami, tom 5. Edukacja przyrodnicza w szkole podstawowej, gimnazjum i liceum. Załącznik do rozporządzenia Ministra Edukacji Narodowej z 23 grudnia 2008 roku w sprawie podstawy programowej wychowania przedszkolnego oraz kształcenia ogólnego w poszczególnych typach szkół z komentarzem.
4. L. Jones, P. Atkins, Chemia ogólna. Cząsteczki, materia, reakcje. s.387, PWN, Warszawa 2006
(1) Zapis oddawanych elektronów w procesie utleniania po stronie substratów ze znakiem ‘-‘ stanowi zapis alternatywny traktowany równorzędnie z podanym.



