Pierwsza grupa układu okresowego, czyli grupa litowców obejmuje takie pierwiastki jak lit, sód, potas, rubid, cez i frans. Wszystkie litowce to metale o barwie srebrzystobiałej, jednak w atmosferze powietrza ulegają zmatowieniu na sutek pokrycia się warstwą tlenku. Z tego powodu metale te przechowuje się w nafcie. Litowce odznaczają się dużą aktywnością chemiczną o której decyduje łatwość oddawania elektronu walencyjnego. Aktywność pierwiastków rośnie w grupie wraz ze wzrostem liczby atomowej (Bielański, 2010).
Wszystkie litowce reagują z wodą. Ze względu na ujemne potencjały standardowe wszystkich litowców redukują one wodór w wodzie zgodnie z równaniem:
2M + 2H2O → 2MOH + H2 ↑
gdzie M to pierwiastek I grupy.
W wyniku reakcji powstaje gazowy wodór i roztwór wodorotlenku litowca.
Sód dodany do krystalizatora z wodą pływa po jej powierzchni, ponieważ jest to metal o gęstości mniejszej od wody. Podczas reakcji wydziela się ciepło, które powoduje stopienie metalu i uformowanie kulki. Fenoloftaleina zabarwia się na kolor malinowy pod wpływem powstającej zasady sodowej.
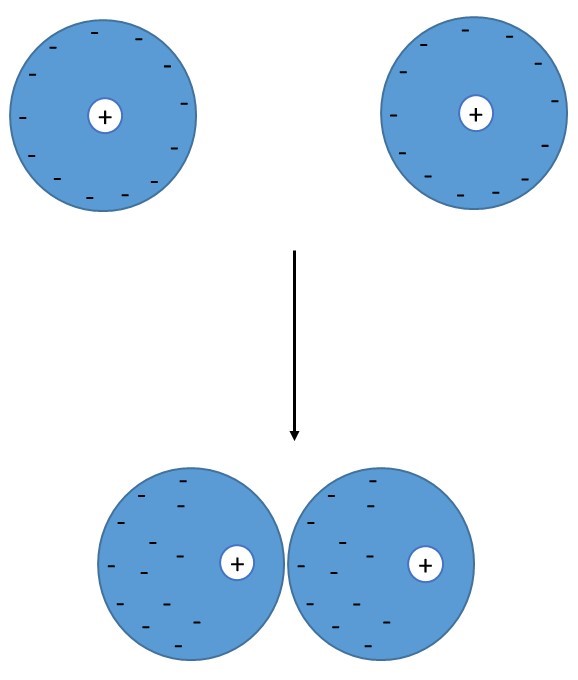
Sód w bardzo ciekawy sposób reaguje z ograniczoną ilością wody. Proces ten został opisany dopiero w styczniu 2015 roku przez czeskich naukowców (Mason & all, 2015) . Okazuje się, że reakcja w pewnych warunkach może zachodzić wybuchowo, a moc eksplozji jest większa niż eksplozja TNT o tej samej masie (Commander, 1975). Dzięki wykorzystaniu ultraszybkich kamer (ponad 11000 fps) udało się zaobserwować, że podczas zetknięcia się kropli wody z powierzchnią metalu natychmiast uwalniane są elektrony z jego powierzchni, obserwowane są powstające iskry. Efekt ten nazwano eksplozją kulombowską.
UWAGA! Substancje niebezpieczne:
Literatura
Bielański, A., 2010. Podstawy Chemii Nieorganicznej. szóste red. Warszawa: PWN.
Commander, J. C. 1975 An explosive hazard analysis of the eutectic solution of NaK and KO2. Nucl. Sci. Abstracts 32, 21922
Mason P. E., Uhlig F., Vaněk V., Buttersack T., Bauerecker S., Jungwirth P. 2015 Coulomb explosion during the early stages of the reaction of alkali metals with water Nature Chemistry Vol 7, 250-254 DOI: 10.1038/NCHEM.2161